搜索


近日,6165cc金沙总站微生物代谢国家重点实验室、6165cc金沙总站李荣秀教授团队在TNF-α疫苗研究方向取得突破进展,研究成果“A Rationally Designed TNF-α Epitope-Scaffold Immunogen Induces Sustained Antibody Response and Alleviates Collagen-Induced Arthritis in Mice”发表于Plos one,并被著名风湿病免疫杂志Nature review rheumatology以“Paving the way for TNF vaccines”为题在Research highlight版块进行专门报道。
TNF-α生物抑制剂是最早用于治疗类风湿关节炎的细胞因子靶点,其在全球生物制剂的销售额一直保持领先地位,但是TNF-α生物抑制剂昂贵的价格和抗药抗体的副作用限制了其广泛的使用。另一种比较好的替代方法,TNF-α疫苗的研制尽管在前期动物实验中显示了良好的效果,但在临床实验中却没有达到预期疗效。设计和研制更加有效的疫苗势在必行。
TNF-α作为人体自身蛋白,要想产生针对其有效的抗体,需要借助安全有效的载体蛋白突破自身免疫耐受。李荣秀课题组经过论证最终选定白喉毒素的转膜结构域DTT作为内源性靶点的载体蛋白。该结构域具有“α螺旋-环状”的特征,结构稳定,可以作为外源表位移植的骨架蛋白,同时其拥有丰富的通用T辅助表位,可以协助自身蛋白打破免疫耐受,为该团队首次报道基于临床已经上市CRM197载体蛋白的有效部位的重新开发利用,保证了其安全有效性;TNF-α有效表位移植到DTT上的疫苗设计,不仅可以在大肠杆菌中高效表达,并且单个表位的应用也避免了TNF-α本身的毒性,为临床应用提供可能。
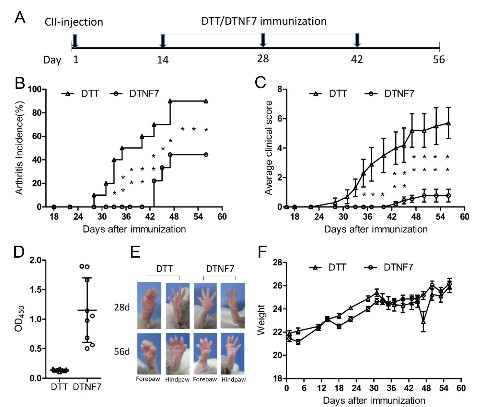
研究人员在CIA小鼠关节炎模型中测试了该疫苗的治疗效果,发现相比于对照组(DTT)可以明显推迟关节炎的发病15天,最终有90%的关节炎模型小鼠发病而DTT对照组仅有45%发病。令人意外的是,该疫苗产生的针对天然TNF-α的特异性抗体可以维持长达6个月的时间,并且几乎绝大多数抗体为IgG1型抗体,相比于对于其他在研疫苗针对的效果具有显著的进步,对类风湿关节炎这种慢性炎症性疾病的治疗也具有明显优势。研究团队目前正在继续开展该疫苗的临床前研究工作并且希望早日进入临床实验。


 首页
首页

 学院概况
学院概况

 师资队伍
师资队伍

 人才培养
人才培养

 招生就业
招生就业

 科学研究
科学研究

 平台基地
平台基地

 党群工作
党群工作

 校友之家
校友之家

 安全工作
安全工作

 网上办事
网上办事

 当前位置:
当前位置: